Sabéis que mutaciones en el gen SCN1A, el cual lleva la información para la síntesis del canal de sodio Nav1.1, esencial para el correcto funcionamiento del cerebro, causan trastornos epilépticos que van desde una forma benigna de epilepsia genética, el GEFS+, hasta una la severa encefalopatía epiléptica del desarrollo que es el síndrome de Dravet. El que la mutación en SCN1A se presente en todas las células del cuerpo o solo en algunas, y/o el que la mutación genere una proteína Nav1.1 funcional pero defectuosa o completamente carente de función, determinará el grado de severidad de la enfermedad.
Sin embargo, aun se desconoce por qué mutaciones similares en SCN1A causan fenotipos (síntomas) variados en los pacientes.
Para explicar esto, se barajan hipótesis no excluyentes como el efecto de la epigenética [modificaciones en la expresión de un gen causadas por alteraciones heredables que no son mutaciones, como por ejemplo un mayor grado de condensación de la cromatina (forma en la que se presenta el ADN en el núcleo celular; la cromatina condensada forma los cromosomas), que impida el acceso al gen de la maquinaria molecular encargada de su expresión] o la presencia de genes modificadores genes que afectan la expresión de otros genes). En este último caso, se han descrito ya algunos genes (ej. genes para receptores GABA o para canales de calcio, cloruro o potasio) con el potencial de modificar la expresión de SCN1A en ratones con síndrome de Dravet.
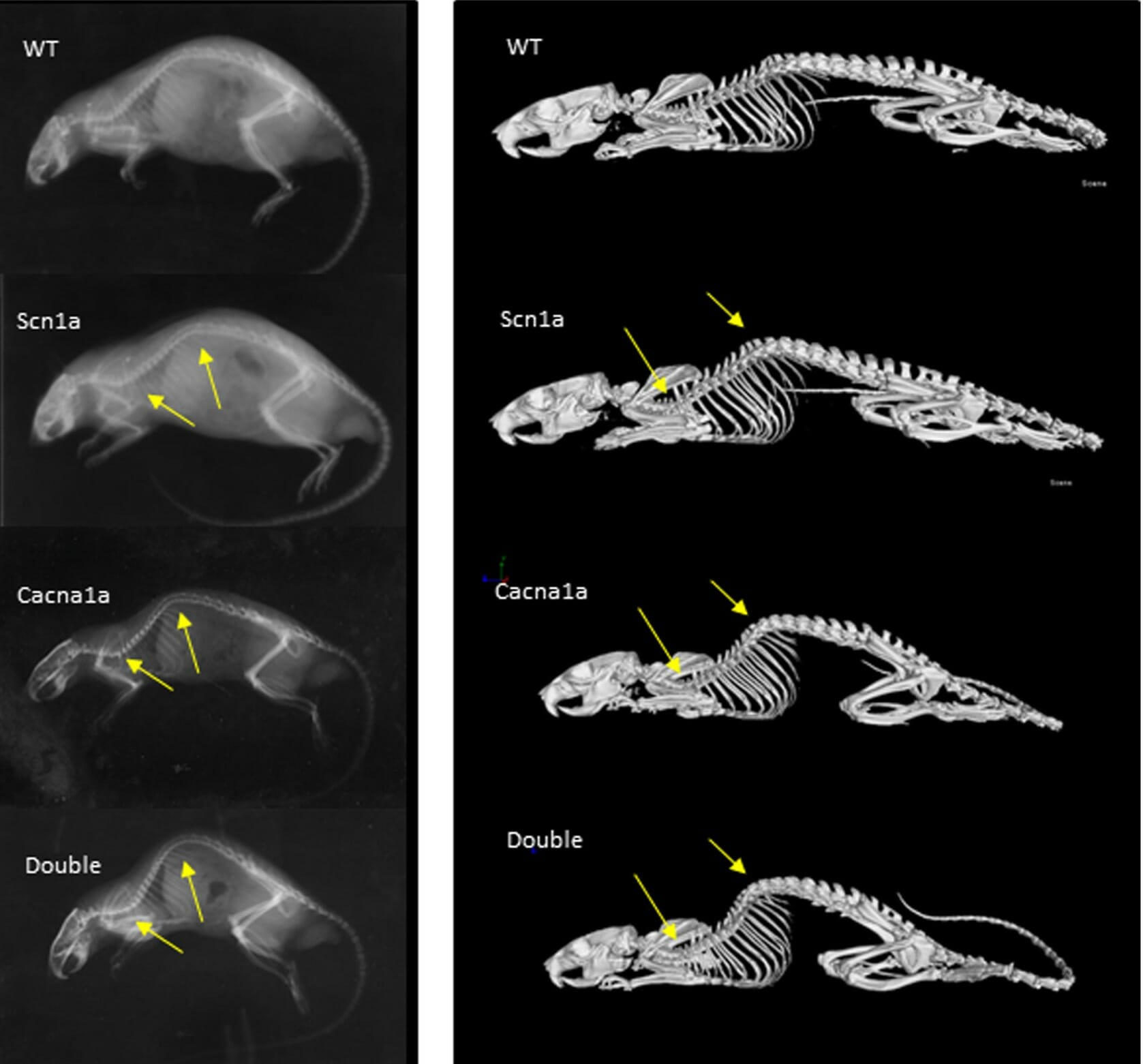
Un estudio reciente se ha centrado en analizar el efecto de la mutación de CACNA1A, un gen que codifica para el canal de calcio Cav2.1 y considerado como posible modificador de SCN1A, en ratas que presentan otra mutación en SCN1A. Ambos genes se expresan en las neuronas específicamente afectadas en pacientes con síndrome de Dravet, las interneuronas parvalbúmina.
Aquí os resumimos los resultados:





Este trabajo pone en evidencia la importancia de utilizar técnicas de secuenciación de nueva generación, con las que se pueden analizar grandes cantidades de material genético, o incluso el genoma completo, en el estudio de pacientes con enfermedades genéticas.
Aunque con limitaciones puesto que aun queda mucho por conocer acerca de los efectos de la epigenética y los genes modificadores en el Dravet, el estudio genético detallado puede ayudar a identificar las causas de los síntomas que padece un paciente. Un diagnóstico genético correcto y completo ayudará a mejorar la estrategia terapéutica del paciente, con el beneficio físico, emocional y económico que esto conlleva para el paciente, la familia y el sistema sanitario.
Podéis leer el estudio, en inglés, AQUÍ.
Un sueño, una meta.